

Sila skupljanja bilo koje jedinične duljine na površini tekućine naziva se površinska napetost, a jedinica je N. · M-1.

Svojstvo smanjenja površinske napetosti otapala naziva se površinska aktivnost, a tvar s ovim svojstvom naziva se površinski aktivna tvar.
Površno aktivna tvar koja može vezati molekule u vodenoj otopini i tvore micele i druge asocijacije, a ima i visoku površinsku aktivnost, a istovremeno ima utjecaja vlaženja, emulgiranja, pjevanja, pranja itd.
Surfaktant su organski spojevi s posebnom strukturom i svojstvom, koji mogu značajno promijeniti interfacijalnu napetost između dvije faze ili površinske napetosti tekućine (uglavnom vode), s vlaženjem, pjevanjem, emulgiranjem, pranjem i drugim svojstvima.
U pogledu strukture, površinski aktivne tvari imaju zajedničko obilježje u tome što sadrže dvije skupine različite prirode u svojim molekulama. Na jednom je kraju dugačak lanac nepolarne skupine, topiv u nafti i netopljivo u vodi, također poznat kao hidrofobna skupina ili vodno-repelentna skupina. Takva vodna skupina za povrat vode općenito je dugi lanci ugljikovodika, ponekad i za organski fluor, silicij, organofosfat, lanac organotina itd. Na drugom kraju je grupa topiva u vodi, hidrofilna skupina ili skupina za povrat nafte. Hidrofilna skupina mora biti dovoljno hidrofilna da bi se osiguralo da su cijeli površinski aktivni tvari topljivi u vodi i da ima potrebnu topljivost. Budući da površinski aktivne tvari sadrže hidrofilne i hidrofobne skupine, mogu biti topive u barem jednoj od tekućih faza. Ovo hidrofilno i lipofilno svojstvo površinski aktivne tvari naziva se amfifilnošću.


Surfaktant je vrsta amfifilnih molekula s hidrofobnim i hidrofilnim skupinama. Hidrofobne skupine površinski aktivnih tvari uglavnom se sastoje od ugljikovodika dugog lanca, poput alkil C8 ~ C20 ravnog lanca, alkil C8 ~ C20 razgranatih lanca (alkilfenil (broj alkil ugljika je 8 ~ 16) i slično. Razlika koja je mala između hidrofobnih skupina uglavnom je u strukturnim promjenama ugljikovodičnih lanaca. A vrste hidrofilnih skupina su više, pa su svojstva površinski aktivnih tvari uglavnom povezana s hidrofilnim skupinama, osim veličine i oblika hidrofobnih skupina. Strukturne promjene hidrofilnih skupina veće su od onih hidrofobnih skupina, tako da se klasifikacija površinski aktivnih tvari uglavnom temelji na strukturi hidrofilnih skupina. Ova se klasifikacija temelji na tome je li hidrofilna skupina ionska ili ne, i podijeljena je na anionske, kationske, neionske, zwitterionske i druge posebne vrste površinski aktivnih tvari.

① Adsorpcija površinski aktivnih tvari na interfacu
Molekule surfaktanata su amfifilne molekule koje imaju i lipofilne i hidrofilne skupine. Kad se površinski aktivno tvar otopi u vodi, njegova hidrofilna skupina privlači vodu i otapa se u vodi, dok se njegova lipofilna skupina odbija vodom i ostavlja vodu, što rezultira adsorpcijom molekula surfaktanata (ili iona) na sučelju dviju faza, što smanjuje međufaktivno napetost između dviju pHaze. Što se više molekula surfaktanata (ili iona) adsorbira na sučelju, to je veće smanjenje interfacijalne napetosti.
② Neka svojstva adsorpcijske membrane
Površinski tlak adsorpcijske membrane: adsorpcija površinski aktivne tvari na sučelju plinske tekućine kako bi se formirala adsorpcijska membrana, poput postavljanja plutajućeg lima bez trenja na sučelju, plutajući lim gura adsorbentnu membranu duž površine otopine, a membrana je na pod tlaka.
Površinska viskoznost: Poput površinskog tlaka, površinska viskoznost je svojstvo koje pokazuje netopljiva molekularna membrana. Ovjeren finim metalnim žičanim platinastim prstenom, tako da njegova ravnina kontaktira vodenu površinu spremnika, okrenite platinasti prsten, platinski prsten viskoznošću prepreke vode, amplituda postupno propada, prema kojem se može mjeriti površinska viskoznost. Metoda je: Prvo se eksperiment provodi na površini čiste vode za mjerenje propadanja amplitude, a zatim se mjeri propadanje nakon stvaranja površinske membrane, a viskoznost površinske membrane izvedena je iz razlike između dva.
Površinska viskoznost usko je povezana s čvrstoćom površinske membrane, a budući da adsorpcijska membrana ima površinski tlak i viskoznost, mora imati elastičnost. Što je veći površinski tlak i veća je viskoznost adsorbirane membrane, to je viši njegov elastični modul. Elastični modul površinske adsorpcijske membrane važan je u procesu stabilizacije mjehurića.
③ Formiranje micela
Razrijeđene otopine površinski aktivnih tvari pridržavaju se zakona praćenih idealnim rješenjima. Količina površinski aktivne tvari adsorbiranim na površini otopine povećava se s koncentracijom otopine, a kada koncentracija dosegne ili prelazi određenu vrijednost, količina adsorpcije više se ne povećava, a ove viška molekule površinski aktivnih tvari su u otopini na neobičan način ili na neki redoviti način. I praksa i teorija pokazuju da formiraju asocijacije u rješenju, a te se udruge nazivaju micele.
Kritična koncentracija micele (CMC): Minimalna koncentracija pri kojoj površinski aktivni tvari tvore micele u otopini naziva se kritična koncentracija micele.
④ CMC vrijednosti uobičajenih površinski aktivnih tvari.

HLB je kratica hidrofilne ravnoteže lipofila, što ukazuje na hidrofilnu i lipofilnu ravnotežu hidrofilne i lipofilne skupine površinski aktivnih tvari, tj. Vrijednost HLB -a površinski aktivne tvari. Velika vrijednost HLB -a ukazuje na molekulu s jakom hidrofilnošću i slabom lipofilnosti; Suprotno tome, snažna lipofilnost i slaba hidrofilnost.
① odredbe vrijednosti HLB -a
Vrijednost HLB-a je relativna vrijednost, tako da kada je vrijednost HLB razvijena, kao standard, vrijednost HLB parafinskog voska, koji nema hidrofilna svojstva, navedena je da je 0, dok je vrijednost HLB natrijevog dodecil sulfata, što je općenito više od vode, u roku od HLB-a. su lipofilni, dok su oni veći od 10 hidrofilni. Dakle, prekretnica od lipofilne do hidrofilne je oko 10.
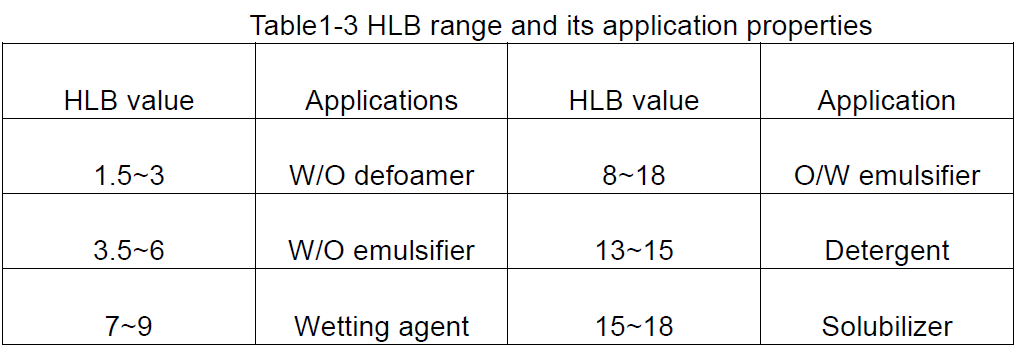
Na temelju vrijednosti HLB-a površinski aktivnih tvari, može se dobiti opća ideja o njihovim mogućim uporabama, kao što je prikazano u tablici 1-3.

Dvije uzajamno netopljive tekućine, jedna se raspršena u drugoj, jer čestice (kapljice ili tekući kristali) tvore sustav nazvan emulzija. Ovaj je sustav termodinamički nestabilan zbog povećanja graničnog područja dviju tekućina kada se formira emulzija. Da bi emulzija postala stabilna, potrebno je dodati treću komponentu - emulgator kako bi se smanjila interfacijalna energija sustava. Emulgator pripada površinski aktivnoj tvari, njegova glavna funkcija je igrati ulogu emulzije. Faza emulzije koja postoji kao kapljica naziva se raspršena faza (ili unutarnja faza, diskontinuirana faza), a druga faza koja je povezana zajedno naziva se disperzijski medij (ili vanjska faza, kontinuirana faza).
① emulgatori i emulzije
Uobičajene emulzije, jedna faza je voda ili vodena otopina, druga faza su organske tvari koje se ne miješa vodom, poput masti, voska itd. Emulzija formirana vodom i uljem može se podijeliti u dvije vrste prema njihovoj disperzijskoj situaciji: nafta raspršena u vodi u obliku ulja, izražena kao em-u uljem, ulje): (voda/ulje). Također se mogu formirati složena voda-u-ulja u/W/W i ulja u ulju u ulju O/W/O tipa multi-emulzije također se mogu formirati.
Emulgatori se koriste za stabilizaciju emulzija smanjenjem interfacijalne napetosti i formiranjem interfacijalne membrane s jednom molekulom.
U emulgiranju zahtjeva emulgatora:
O: Emulgator mora biti u stanju adsorbirati ili obogatiti sučelje između dvije faze, tako da se smanjuje interfacijalna napetost;
B: Emulgator mora dati čestice naboju, tako da elektrostatičko odboj između čestica ili tvori stabilnu, visoko viskoznu zaštitnu membranu oko čestica.
Stoga, tvar koja se koristi kao emulgator mora imati amfifilne skupine kako bi se emulgirali, a površinski aktivne tvari mogu ispuniti ovaj zahtjev.
② Metode pripreme emulzija i čimbenika koji utječu na stabilnost emulzija
Postoje dva načina za pripremu emulzija: jedan je koristiti mehaničku metodu za rastjerivanje tekućine u sitnim česticama u drugoj tekućini, koja se u industriji uglavnom koristi za pripremu emulzija; Drugi je otopiti tekućinu u molekularnom stanju u drugoj tekućini, a zatim je pravilno okupljati kako bi se formirala emulzija.
Stabilnost emulzije je sposobnost agregacije protiv čestica koja dovodi do odvajanja faze. Emulzije su termodinamički nestabilni sustavi s velikom slobodnom energijom. Stoga je takozvana stabilnost emulzije zapravo vrijeme potrebno da sustav dostigne ravnotežu, tj. Vrijeme potrebno za odvajanje jedne od tekućine u sustavu.
Kada je interfacijalna membrana s masnim alkoholima, masnim kiselinama i masnim aminima i drugim polarnim organskim molekulama, čvrstoća membrane značajno veća. To je zato što se u međufaznom adsorpcijskom sloju molekula i alkohola emulgatora i alkohola, kiselina i amini i druge polarne molekule da bi tvorili "kompleks", tako da se povećala snaga interfacijalne membrane.
Emulgatori koji se sastoje od više od dva površinski aktivnih tvari nazivaju se miješanim emulgatorima. Mješoviti emulgator adsorbiran na sučelju vode/ulja; Intermolekularno djelovanje može tvoriti komplekse. Zbog snažnog intermolekularnog djelovanja, interfacijalna napetost se značajno smanjuje, količina emulgatora adsorbiranog na sučelju značajno se povećava, stvaranje gustoće interfacijalne membrane raste, jačina se povećava.
Naboj tekućih perlica ima značajan utjecaj na stabilnost emulzije. Stabilne emulzije, čije su tekuće kuglice općenito naplaćene. Kada se koristi ionski emulgator, ion emulgatora adsorbiran na sučelju ima svoju lipofilnu skupinu umetnutu u uljnu fazu, a hidrofilna skupina je u vodenoj fazi, čime se tekuće perle napune. Kako se emulzijske perle s istim nabojem, oni se odbijaju, ne lako se aglomeriraju, tako da se stabilnost povećava. Može se vidjeti da što se više iona emulgatora adsorbira na zrncama, to je veća naboj, veća je sposobnost da se perlice spriječe aglomeraciju, to je stabilniji sustav emulzije.
Viskoznost medija za disperziju emulzije ima određeni utjecaj na stabilnost emulzije. Općenito, što je veća viskoznost disperzijskog medija, veća je stabilnost emulzije. To je zato što je viskoznost disperzijskog medija velika, što ima snažan učinak na Brownovo gibanje tekućih perlica i usporava sudar između tekućih perlica, tako da sustav ostaje stabilan. Obično polimerne tvari koje se mogu otopiti u emulzijama mogu povećati viskoznost sustava i povećati stabilnost emulzija. Osim toga, polimeri također mogu formirati snažnu interfacijalnu membranu, čineći sustav emulzije stabilnijim.
U nekim slučajevima, dodavanje čvrstog praha također može učiniti da se emulzija stabilizira. Čvrsti prah nalazi se u vodi, ulju ili sučelju, ovisno o ulju, voda na vježbi čvrstog praha, ako čvrsti prah nije potpuno vlažan s vodom, ali također vlažan uljem, ostat će na sučelju vode i ulja.
Čvrsti prah ne čini emulziju stabilnom jer prah prikupljen na sučelju pojačava interfacijalnu membranu, što je slično interfacijalnoj adsorpciji molekula emulgatora, pa što je čvrsti materijal u prahu raspoređen na sučelju, to je stabilnija emulzija.
Surfaktanti imaju mogućnost značajnog povećanja topljivosti netopljivih ili blago topivih organskih tvari nakon formiranja micela u vodenoj otopini, a otopina je u ovom trenutku transparentna. Taj se učinak micele naziva solubilizacija. Surfaktant koji može proizvesti solubilizaciju naziva se solubilizator, a organska tvar koja je solubilizirana naziva se solubilizirana tvar.

Pjena igra važnu ulogu u procesu pranja. Pjena je disperzijski sustav u kojem se plin raspršuje u tekućoj ili krutici, s plinom kao raspršena faza i tekućina ili kruta kao medij za raspršivanje, a prva se naziva tekuća pjena, dok se drugi naziva čvrsta pjena, poput pjenastih plastika, pjenastog stakla, pjenastog cementa itd.
(1) Formiranje pjene
Pod pjenom mislimo ovdje na agregat mjehurića zraka odvojenih tekućim membranom. Ova vrsta mjehurića uvijek se brzo diže do tekuće površine zbog velike razlike u gustoći između raspršene faze (plina) i disperzijskog medija (tekućina), u kombinaciji s niskom viskoznošću tekućine.
Proces formiranja mjehurića je unijeti veliku količinu plina u tekućinu, a mjehurići u tekućini brzo se vraćaju na površinu, formirajući agregat mjehurića odvojenih malom količinom tekućeg plina.
Pjena ima dvije značajne karakteristike u smislu morfologije: jedan je da su mjehurići kao raspršena faza često poliedarski oblik, to je zato što je na sjecištu mjehurića tanko tendencija da se tekući film tanak tako da mjehurići postanu poliedral, kada tekući film u određenoj mjeri dovodi do rupture mjehurića; Drugo je da čiste tekućine ne mogu formirati stabilnu pjenu, tekućina koja može oblikovati pjenu je najmanje dvije ili više komponenti. Vodene otopine površinski aktivnih tvari tipični su za sustave koji su skloni stvaranju pjene, a njihova sposobnost stvaranja pjene također je povezana s drugim svojstvima.
Surfaktanti s dobrom snagom pjene nazivaju se pjenastim sredstvima. Iako sredstvo za pjevanje ima dobru sposobnost pjene, ali formirana pjena možda neće moći dugo održavati, odnosno, njegova stabilnost nije nužno dobra. Da bi se održala stabilnost pjene, često u sredstvom za pjevanje kako bi dodala tvari koje mogu povećati stabilnost pjene, tvar se naziva stabilizator pjene, obično se koristi stabilizator lauril dietanolamin i dodecil dimetilamin oksid.
(2) Stabilnost pjene
Pjena je termodinamički nestabilan sustav, a konačni trend je da se ukupna površina tekućine unutar sustava smanjuje nakon što se mjehurić razbije, a slobodna energija opada. Proces depoaminga je postupak kojim tekuća membrana koja razdvaja plin postaje gušća i tanja dok se ne pokvari. Stoga se stupanj stabilnosti pjene uglavnom određuje brzinom tekućeg pražnjenja i čvrstoćom tekućeg filma. Sljedeći čimbenici također utječu na to.
(3) Uništavanje pjene
Osnovni princip uništavanja pjene je promijeniti uvjete koji proizvode pjenu ili uklanjanje stabilizacijskih čimbenika pjene, pa postoje i fizičke i kemijske metode depoaminga.
Fizičko defoaming znači promjenu uvjeta proizvodnje pjene uz održavanje kemijskog sastava otopine pjene, poput vanjskih poremećaja, promjena temperature ili tlaka i ultrazvučnog tretmana učinkovite fizičke metode za uklanjanje pjene.
Metoda kemijske depoacije je dodavanje određenih tvari za interakciju s sredstvom za pjenjenje kako bi se smanjila čvrstoća tekućeg filma u pjeni i na taj način smanjila stabilnost pjene kako bi se postigla svrha depoaminga, takve se tvari nazivaju depoamerima. Većina depoatora su površinski aktivne tvari. Stoga, prema mehanizmu depoaminga, depoamer bi trebao imati snažnu sposobnost smanjenja površinske napetosti, lako se adsorbirati na površini, a interakcija između molekula površinske adsorpcije je slaba, adsorpcijske molekule raspoređene u olalosnijoj strukturi.
Postoje razne vrste depoamer-a, ali u osnovi su sve to neionske površinski aktivne tvari. Neionske površinski aktivne tvari imaju svojstva protiv iscrpljivanja u blizini ili iznad svoje točke oblaka i često se koriste kao depoameri. Alkoholi, posebno alkoholi s granastom strukturom, masnim kiselinama i esterima masnih kiselina, poliamida, fosfatnih estera, silikonskih ulja itd. Također se obično koriste kao izvrsni depoameri.
(4) Pjena i pranje
Ne postoji izravna veza između pjene i učinkovitosti pranja, a količina pjene ne ukazuje na učinkovitost pranja. Na primjer, neionski površinski aktivni tvari imaju daleko manje svojstava pjene od sapuna, ali njihova je dekontaminacija mnogo bolja od sapuna.
U nekim slučajevima, pjena može biti od pomoći u uklanjanju prljavštine i prljavštine. Na primjer, prilikom pranja posuđa u kući, pjena deterdženta uzima kapljice ulja i prilikom pročišćavanja tepiha, pjena pomaže u pokupu prašine, praha i druge čvrste prljavštine. Pored toga, pjena se ponekad može koristiti kao pokazatelj učinkovitosti deterdženta. Budući da masna ulja imaju inhibicijski učinak na pjenu deterdženta, kada je previše ulja i premalo deterdženta, neće se stvoriti pjena ili će originalna pjena nestati. Pjena se ponekad može koristiti i kao pokazatelj čistoće ispiranja, jer količina pjene u otopini za ispiranje obično se smanjuje sa smanjenjem deterdženta, tako da se količina pjene može koristiti za procjenu stupnja ispiranja.
U širokom smislu, pranje je postupak uklanjanja neželjenih komponenti iz objekta koji se pere i postiže neke svrhe. Pranje u uobičajenom smislu odnosi se na postupak uklanjanja prljavštine s površine nosača. U ispiranju interakcija između prljavštine i nosača oslabi ili eliminira djelovanjem nekih kemijskih tvari (npr. Deterdženta itd.), Tako da se kombinacija prljavštine i nosača promijeni u kombinaciju prljavštine i deterdženta, a na kraju je prljavština odvojena od nosača. Budući da su predmeti koji se mogu oprati i uklanjaju prljavština raznolika, pranje je vrlo složen proces i osnovni postupak pranja može se izraziti u sljedećim jednostavnim odnosima.
Carrie ·· prljavština + deterdžent = nosač + prljavština · deterdžent
Proces pranja obično se može podijeliti u dvije faze: prvo, pod djelovanjem deterdženta, prljavština je odvojena od njegovog nosača; Drugo, odvojena prljavština se raspršuje i suspendira u mediju. Postupak pranja je reverzibilan postupak, a prljavština se raspršila i suspendirana u mediju također može ponovno precipitirati iz medija na objekt koji se ispire. Stoga bi dobar deterdžent trebao imati mogućnost rastjerivanja i suspendiranja prljavštine i spriječiti ponovnu jedinicu prljavštine, osim mogućnosti uklanjanja prljavštine s nosača.
(1) Vrste prljavštine
Čak i za istu stavku, vrsta, sastav i količina prljavštine mogu varirati ovisno o okruženju u kojem se koristi. Prljavština naftnog tijela uglavnom je neka životinjska i biljna ulja i mineralna ulja (poput sirove nafte, loživog ulja, ugljenog katrana itd.), Čvrsta prljavština je uglavnom čađa, pepeo, hrđa, ugljična crna itd. U smislu odjeće, prljavština je iz ljudskog tijela, poput znoja, sebuma, krvi, itd.; Prljavština od hrane, poput mrlja od voća, mrlje za ulje za kuhanje, mrlje začina, škrob itd.; prljavština iz kozmetike, poput ruževa, laka za nokte itd.; Prljavština iz atmosfere, poput čađe, prašine, blata itd.; Drugi, poput tinte, čaja, premaza itd. Dolazi u raznim vrstama.
Različite vrste prljavštine obično se mogu podijeliti u tri glavne kategorije: čvrsta prljavština, tekuća prljavština i posebna prljavština.
① Čvrsta prljavština
Uobičajena čvrsta prljavština uključuje čestice pepela, blata, zemlje, hrđe i ugljikovog crne boje. Većina ovih čestica ima električni naboj na površini, većina ih je negativno nabijena i može se lako adsorbirati na predmete vlakana. Čvrstu prljavštinu općenito je teško otapati u vodi, ali se može raspršiti i suspendirati otopinama deterdženata. Čvrstu prljavštinu s manjom točkom mase teže je ukloniti.
② Tekuća prljavština
Tekuća prljavština uglavnom je topiva u ulju, uključujući biljna i životinjska ulja, masne kiseline, masne alkohole, mineralna ulja i njihove okside. Među njima se mogu pojaviti biljna i životinjska ulja, masne kiseline i alkalna saponifikacija, dok masni alkoholi, mineralna ulja nisu saponificirana alkalijama, već mogu biti topiva u alkoholima, etirima i organskim otapalima ugljikovodika, a emulziranje i disperziranje vode u deterdginju. Tekuća prljavština topiva nafta uglavnom ima snažnu silu s predmetima vlakana i čvršće se adsorbira na vlaknima.
③ Posebna prljavština
Posebna prljavština uključuje proteine, škrob, krv, ljudske izlučevine poput znoja, sebuma, urina i voćnog soka i soka čaja. Većina ove vrste prljavštine može se kemijski i snažno adsorbirati na predmete vlakana. Stoga je teško oprati.
Različite vrste prljavštine rijetko se nalaze same, ali se često miješaju i adsorbiraju na objekt. Prljavština se ponekad može oksidirati, raspadati ili raspadati pod vanjskim utjecajima, stvarajući tako novu prljavštinu.
(2) Privršenost prljavštine
Odjeća, ruke itd. Mogu se obojiti jer postoji neka vrsta interakcije između predmeta i prljavštine. Prljavština se pridržava predmeta na različite načine, ali nema više od fizičkih i kemijskih adhezija.
① Prianjanje čađe, prašine, blata, pijeska i ugljena do odjeće fizička je adhezija. Općenito govoreći, kroz ovu adheziju prljavštine i uloga između obojenog objekta relativno je slaba, uklanjanje prljavštine je također relativno jednostavno. Prema različitim silama, fizička adhezija prljavštine može se podijeliti u mehaničku adheziju i elektrostatičku adheziju.
O: Mehanička adhezija
Ova vrsta adhezije uglavnom se odnosi na adheziju neke čvrste prljavštine (npr. Prašina, blato i pijesak). Mehanička adhezija jedan je od slabijih oblika adhezije prljavštine i može se ukloniti gotovo čisto mehaničkim sredstvima, ali kada je prljavština mala (<0,1UM), to je teže ukloniti.
B: Elektrostatička prianjanje
Elektrostatička adhezija uglavnom se očituje u djelovanju nabijenih čestica prljavštine na suprotno nabijenim objektima. Većina vlaknastih predmeta negativno se nabija u vodi i može se lako pridržavati određenim pozitivno nabijenim prljavštima, poput tipova vapna. Neka prljavština, iako negativno nabijena, poput čestica ugljičnih crnaca u vodenim otopinama, može se pridržavati vlakana kroz ionske mostove (ioni između višestruko nabijenih predmeta, djelujući zajedno s njima na mostov način) nastale pozitivnim ionima u vodi (npr. Ca2+ , mg2+ itd.).
Elektrostatičko djelovanje je jače od jednostavnog mehaničkog djelovanja, što uklanjanje prljavštine relativno teže.
② Kemijska adhezija
Kemijska adhezija odnosi se na fenomen prljavštine koja djeluje na objekt kemijskim ili vodikovim vezama. Na primjer, polarna čvrsta prljavština, protein, hrđa i druga adhezija na vlaknima, vlakna sadrže karboksil, hidroksil, amid i druge skupine, ove skupine i masne masne kiseline, masni alkoholi lako se formiraju vodikove veze. Kemijske sile su općenito jake i prljavština je stoga čvršće vezana za objekt. Ovu vrstu prljavštine teško je ukloniti uobičajenim metodama i zahtijevaju posebne metode da se s njom nose.
Stupanj prianjanja prljavštine povezan je s prirodom same prljavštine i prirodom objekta kojem se pridržava. Općenito, čestice se lako pridržavaju vlaknastih predmeta. Što je manja tekstura čvrste prljavštine, to je jača adhezija. Polarna prljavština na hidrofilnim predmetima kao što su pamuk i staklo pridržavaju se snažnije od nepolarne prljavštine. Nepolarna prljavština se drži snažnije od polarne prljavštine, poput polarnih masti, prašine i gline, a manje je lako ukloniti i čistiti.
(3) Mehanizam za uklanjanje prljavštine
Svrha pranja je uklanjanje prljavštine. U mediju određene temperature (uglavnom vode). Korištenje različitih fizičkih i kemijskih učinaka deterdženta kako bi oslabili ili eliminirali učinak prljavštine i ispranih predmeta, pod djelovanjem određenih mehaničkih sila (poput trljanja ruku, agitacije perilice rublja, utjecaja vode), tako da su prljavština i isprani predmeti iz svrhe dekontaminacije.
① Mehanizam uklanjanja tekuće prljavštine
A: Vlaženje
Tečno prljavština je uglavnom na bazi ulja. Ulje mrlja navlaže se najzahtjevnijim predmetima i širi se više ili manje kao uljni film na površini vlaknastog materijala. Prvi korak u akciji pranja je vlaženje površine od tekućine za pranje. Radi ilustracije, površina vlakana može se smatrati glatkom čvrstom površinom.
B: Odvajanje nafte - mehanizam za uvijanje
Drugi korak u postupku pranja je uklanjanje ulja i masti, uklanjanje tekuće prljavštine postiže se vrsta namotavanja. Tekuća prljavština prvotno je postojala na površini u obliku raširenog uljanog filma, a pod preferencijalnim efektom vlaženja tekućine za pranje na čvrstu površinu (tj. Površinu vlakana), uvijena je u uljne kuglice korak po korak, koje je zamijenila tekućina za pranje i na kraju napustila površinu pod određenim vanjskim silama.
② Mehanizam uklanjanja čvrste prljavštine
Uklanjanje tekuće prljavštine uglavnom je kroz preferencijalno vlaženje nosača prljavštine otopinom za pranje, dok je mehanizam za uklanjanje čvrste prljavštine različit, gdje se postupak pranja uglavnom odnosi na vlaženje mase prljavštine i njezine površine nosača otopinom za pranje. Zbog adsorpcije površinski aktivnih tvari na čvrstoj prljavštini i njegove površine nosača, interakcija između prljavštine i površine je smanjena, a čvrstoća adhezije mase prljavštine na površini se smanjuje, pa se masa prljavštine lako uklanja s površine nosača.
Pored toga, adsorpcija površinski aktivnih tvari, posebno ionskih površinski aktivnih tvari, na površini čvrste prljavštine i njegovog nosača ima potencijal povećati površinski potencijal na površini čvrste prljavštine i njegovog nosača, što je pogodnije za uklanjanje prljavštine. Čvrste ili općenito vlaknaste površine obično se negativno naplaćuju u vodenom mediju i stoga mogu formirati difuzne dvostruke elektroničke slojeve na masama prljavštine ili čvrstih površina. Zbog odbijanja homogenih naboja, prianjanje čestica prljavštine u vodi na čvrstu površinu je oslabljena. Kada se doda anionski površinski aktivni tvar, jer može istovremeno povećati negativni površinski potencijal čestice prljavštine i čvrste površine, odbojnost između njih je sve veća, čvrstoća adhezije čestice je sve više smanjena, a prljavština je lakše ukloniti.
Nasinski površinski aktivne tvari adsorbirani su na općenito nabijenim čvrstim površinama i iako ne mijenjaju značajno interfacijalni potencijal, adsorbirani neionski površinski aktivni tvari imaju tendenciju da formiraju određenu debljinu adsorbiranog sloja na površini što pomaže u sprječavanju ponovnog redeliziranja prljavštine.
U slučaju kationskih površinski aktivnih tvari, njihova adsorpcija smanjuje ili eliminira negativni površinski potencijal mase prljavštine i njegove površine nosača, što smanjuje odboj između prljavštine i površine i stoga ne pogoduje uklanjanju prljavštine; Nadalje, nakon adsorpcije na čvrstoj površini, kationski površinski aktivni tvari obično okreću hidrofobnu površinu i stoga ne pogoduju vlaženjem na površinu i stoga pranja.
③ Uklanjanje posebnih tla
Protein, škrob, ljudska izlučevina, voćni sok, sok od čaja i druge takve prljavštine teško je ukloniti normalnim površinski aktivnim tvarima i zahtijevati poseban tretman.
Proteinske mrlje poput vrhnja, jaja, krvi, mlijeka i kože izlučivaju se koaguliraju na vlaknima i degeneraciji i postaju jača adhezija. Proteinsko prljavština može se ukloniti pomoću proteaza. Enzimska proteaza razgrađuje proteine u prljavštini u aminokiseline topive u vodi ili oligopeptide.
Mrlje od škroba uglavnom potječu od namirnica, a drugi poput gravčana, ljepila itd. Amilaza ima katalitički učinak na hidrolizu mrlja od škroba, zbog čega se škrob raspada na šećere.
Lipaza katalizira raspadanje triglicerida, koje je teško ukloniti normalnim metodama, poput sebuma i jestivih ulja, i razbija ih u topljivi glicerol i masne kiseline.
Neke obojene mrlje od voćnih sokova, sokova za čaj, mastila, ruž itd. Često je teško očistiti čak i nakon ponovljenog pranja. Ove mrlje mogu se ukloniti redoks reakcijom oksidirajućim ili redukcijskim agensom kao što je izbjeljivač, koje uništava strukturu skupina koje generiraju boje ili boja i u boji i razgrađuju ih u manje komponente topive u vodi.
(4) Mehanizam za uklanjanje mrlja od kemijskog čišćenja
Navedeno je zapravo za vodu kao medij pranja. U stvari, zbog različitih vrsta odjeće i građevine, neka odjeća koja koristi pranje vode nije prikladna ili nije lako oprati čista, odjeću nakon pranja, pa čak i deformacije, blijede itd., Na primjer: većina prirodnih vlakana apsorbira vodu i lako je nabrijana, a suha i laka za smanjenje, pa će nakon pranja biti deformirana; Pranjenim proizvodima od vune također se često pojavljuju fenomen skupljanja, neki vuneni proizvodi s pranjem vode također su lako pilule, promjenu boje; Neke svile osjećaju se još gore nakon pranja i gube svoj sjaj. Za ovu odjeću često koristi metodu suhog čišćenja za dekontaminaciju. Takozvano kemijsko čišćenje uglavnom se odnosi na metodu pranja u organskim otapalima, posebno u nepolarnim otapalima.
Beho čišćenje je nježniji oblik pranja od pranja vode. Budući da kemijsko čišćenje ne zahtijeva mnogo mehaničkog djelovanja, to ne uzrokuje oštećenje, nabora i deformacije odjeće, dok sredstva za kemijsko čišćenje, za razliku od vode, rijetko stvaraju širenje i kontrakciju. Sve dok se tehnologija pravilno obrađuje, odjeća se može očistiti bez izobličenja, blijede boje i produženog radnog vijeka.
U pogledu kemijskog čišćenja, postoje tri široke vrste prljavštine.
Prljavština od prljavštine od prljavštine od prljavštine uključuje sve vrste ulja i masti, koja je tekuća ili masna i može se otopiti u otapalima za čišćenje.
Prljavština od prljavštine topiva u vodi topiva je topljiva u vodenim otopinama, ali ne i u sredstvima za čišćenje, adsorbira se na odjeći u vodenom stanju, voda isparava nakon nanošenja granularnih krutih tvari, poput neorganskih soli, škroba, proteina, itd.
③Oil i voda netopljivo prljavština i voda netopljiva prljavština nisu topiva u vodi niti topiva u otapala za čišćenje kera, poput ugljične crne boje, silikata različitih metala i oksida, itd.
Zbog različite prirode različitih vrsta prljavštine, postoje različiti načini uklanjanja prljavštine u procesu čišćenja suhog čišćenja. Tla topljiva na ulju, poput životinjskih i biljnih ulja, mineralnih ulja i masti, lako su topiva u organskim otapalima i mogu se lakše ukloniti u kemijskom čišćenju. Izvrsna topljivost otapala za čišćenje suhog čista za ulja i masti u osnovi potječu od sila van der zidova između molekula.
Za uklanjanje prljavštine topive u vodi, poput anorganskih soli, šećera, proteina i znoja, pravoj količini vode također se mora dodati u agens za čišćenje suhog čišćenja, inače je iz odjeće teško ukloniti prljavštinu u vodi. Međutim, vodu je teško rastopiti u srednjem sredstvu za čišćenje, tako da za povećanje količine vode morate dodati i površinski aktivne tvari. Prisutnost vode u sredstvom za čišćenje može učiniti površinu prljavštine i odjeće hidrirane, tako da je lako komunicirati s polarnim skupinama površinski aktivnih tvari, što pogoduje adsorpciji površinski aktivnih tvari na površini. Osim toga, kada površinski aktivne tvari formiraju micele, prljavštinu i voda topiva u vodi mogu se solubilizirati u micele. Osim što povećavaju sadržaj vode u otapalu za suho čišćenje, površinski aktivne tvari također mogu igrati ulogu u sprečavanju ponovnog taloženja prljavštine kako bi se poboljšao učinak dekontaminacije.
Prisutnost male količine vode potrebna je za uklanjanje prljavštine topive u vodi, ali previše vode može uzrokovati izobličenje i nabora u nekoj odjeći, tako da količina vode u agensu za čišćenje suhog čista mora biti umjerena.
Prljavština koja nije topiva u vodi niti topiva ulja, čvrste čestice poput pepela, blata, zemlje i ugljične crne, uglavnom su pričvršćene na odjeću elektrostatičkim silama ili u kombinaciji s uljem. U suhom čišćenju, protok otapala, utjecaj može učiniti elektrostatičku silu adsorpciju prljavštine, a sredstvo za čišćenje suhog čišćenja može otopiti ulje, tako da kombinacija ulja i prljavštine i pričvršćena na odjeću čvrstih čestica u agensu za čišćenje suhog čišćenja, u malom količini vode, tako da su oni bili izgnječani, tako da su oni bili izloženi u silu. odjeća.
(5) Čimbenici koji utječu na radnju pranja
Usmjerena adsorpcija površinski aktivnih tvari na sučelju i smanjenje površinske (interfacijalne) napetosti glavni su čimbenici u uklanjanju tekuće ili čvrste prljavštine. Međutim, postupak pranja je složen, a učinak pranja, čak i s istim vrstom deterdženta, utječu i mnogi drugi čimbenici. Ti čimbenici uključuju koncentraciju deterdženta, temperaturu, prirodu prljavštine, vrstu vlakana i strukturu tkanine.
① Koncentracija surfaktanata
Micele površinski aktivnih tvari u otopini igraju važnu ulogu u procesu pranja. Kad koncentracija dosegne kritičnu koncentraciju micele (CMC), učinak pranja naglo se povećava. Stoga bi koncentracija deterdženta u otapalu trebala biti veća od vrijednosti CMC -a da bi imala dobar učinak pranja. Međutim, kada je koncentracija površinski aktivnih tvari veća od vrijednosti CMC -a, inkrementalno povećanje učinka pranja nije očito i nije potrebno previše povećati koncentraciju površinski aktivnih tvari.
Pri uklanjanju ulja solubilizacijom, učinak solubilizacije povećava se s povećanjem koncentracije površinski aktivne tvari, čak i kada je koncentracija iznad CMC -a. U ovom je trenutku preporučljivo koristiti deterdžent na lokalni centralizirani način. Na primjer, ako na manžetima i ovratniku odjeće ima puno prljavštine, sloj deterdženta može se primijeniti tijekom pranja kako bi se povećao efekt solubilizacije površinski aktivnih tvari na ulje.
②temperatura ima vrlo važan utjecaj na radnju dekontaminacije. Općenito, povećanje temperature olakšava uklanjanje prljavštine, ali ponekad i previsoka temperatura može uzrokovati nedostatke.
Povećanje temperature olakšava difuziju prljavštine, čvrsta mast se lako emulgira na temperaturama iznad njegove tališta, a vlakna povećavaju oticanje zbog povećanja temperature, a sve to olakšava uklanjanje prljavštine. Međutim, za kompaktne tkanine, mikrogapi između vlakana smanjuju se kako se vlakna šire, što je štetno za uklanjanje prljavštine.
Promjene temperature također utječu na topljivost, vrijednost CMC -a i veličinu micele površinski aktivnih tvari, što utječe na učinak pranja. Topljivost površinski aktivnih tvari s dugim ugljikovim lancima je niska na niskim temperaturama, a ponekad je topljivost čak niža od vrijednosti CMC -a, tako da temperaturu pranja treba podići na odgovarajući način. Učinak temperature na vrijednost CMC i veličinu micele različit je za ionske i neionske površinski aktivne tvari. Za ionske površinski aktivne tvari, povećanje temperature općenito povećava vrijednost CMC -a i smanjuje veličinu micele, što znači da bi koncentraciju površinski aktivnog sredstva u otopini za pranje trebalo povećati. Za neionske površinski aktivne tvari, porast temperature dovodi do smanjenja vrijednosti CMC-a i značajnog povećanja volumena micela, tako da je jasno da će odgovarajuće povećanje temperature pomoći neionskom površinski aktivnoj tvari da izvrši svoj površinski aktivni učinak. Međutim, temperatura ne bi trebala premašiti njegovu točku oblaka.
Ukratko, optimalna temperatura pranja ovisi o formulaciji deterdženta i objektu koji se ispire. Neki deterdženti imaju dobar učinak deterdženta na sobnoj temperaturi, dok drugi imaju puno različito deterdžente između hladnog i vrućeg pranja.
③ pjena
Uobičajeno je zbuniti snagu pjene s efektom pranja, vjerujući da deterdženti s visokom snagom pjene imaju dobar učinak pranja. Istraživanje je pokazalo da ne postoji izravan odnos između učinka pranja i količine pjene. Na primjer, pranje s deterdžentima s niskim pjenama nije manje učinkovito od pranja s deterdžentima s visokim pjenama.
Iako pjena nije izravno povezana s pranjem, postoje slučajevi kada pomaže u uklanjanju prljavštine, na primjer, prilikom pranja posuđa ručno. Kada pročišćavaju tepihe, pjena također može oduzeti prašinu i druge čestice čvrste prljavštine, prljavština tepiha čini veliki udio prašine, tako da sredstva za čišćenje tepiha trebaju imati određenu sposobnost pjene.
Snaga pjene također je važna i za šampone, gdje sitna pjena proizvedena od tekućine tijekom šamponiranja ili kupanja ostavlja kosu pod mazivom i udobnom.
④ Sorte vlakana i fizička svojstva tekstila
Uz kemijsku strukturu vlakana, koja utječu na adheziju i uklanjanje prljavštine, pojava vlakana i organizacija pređe i tkanine utječu na lakoću uklanjanja prljavštine.
Vage vunenih vlakana i zakrivljene ravne vrpce pamučnih vlakana vjerojatnije će akumulirati prljavštinu od glatkih vlakana. Na primjer, ugljični crni obojeni na celuloznim filmovima (viskoznim filmovima) lako je ukloniti, dok je ugljično crno obojeno na pamučnim tkaninama teško isprati. Drugi je primjer da su tkanine s kratkim vlaknima izrađene od poliestera sklonije akumulaciji mrlja od ulja od tkanina s dugim vlaknima, a mrlje ulja na tkaninama s kratkim vlaknima također je teže ukloniti mrlje od ulja na tkaninama s dugim vlaknima.
Čvrsto iskrivljene pređe i uske tkanine, zbog malog jaza između vlakana, mogu odoljeti invaziji na prljavštinu, ali iste također mogu spriječiti da tekućina za pranje isključi unutarnju prljavštinu, tako da su teške tkanine počnu odoljeti dobroj prljavštini, ali jednom je i teže obojeno pranje.
⑤ Tvrdoća vode
Koncentracija CA2+, Mg2+ i drugih metalnih iona u vodi ima veliki utjecaj na učinak pranja, posebno kada anionske površinski aktivne tvari naiđu na CA2+ i Mg2+ ioni koji tvore kalcij i magnezijske soli koji su manje topivi i smanjit će njegovo detertno stanje. U tvrdoj vodi, čak i ako je koncentracija površinski aktivnih tvari visoka, deterdženti je i dalje mnogo gore nego u destilaciji. Da bi surfaktant imao najbolji učinak pranja, koncentracija CA2+ iona u vodi treba smanjiti na 1 x 10-6 mol/L (CaCO3 do 0,1 mg/L) ili manje. To zahtijeva dodavanje različitih omekšivača u deterdžent.
Post Vrijeme: veljače-25-2022



